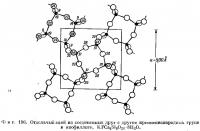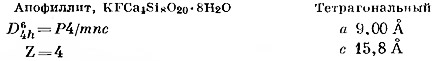
Как уже упоминалось выше (стр. 172), апофиллит построен из слоев определенным образом связанных тетраэдрических групп. Эти слои состоят из тетраэдров, соединенных один с другим тремя вершинами. Как и в случае слюд, слои соответствуют группам Si2O5, входящим в химическую формулу. Слои, однако, не обладают гексагональным мотивом, как в слюдах, но содержат кольца из четырех и восьми тетраэдров. Частично такой слой показан на фиг. 196 в проекции на базальную плоскость (001). Чередующиеся четырехчленные кольца попеременно обращены вершинами тетраэдров вниз и вверх относительно плоскости рисунка. В этих вершинах находятся активные атомы кислорода, соединенные только с одним атомом кремния. К этим атомам кислорода присоединяются катионы.
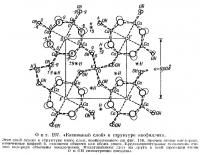
Представим себе, что подобные кремнекислородные сетки наложены одна на другую и связаны слоями катионов, располагающимися в плоскости симметрии. «Слой катионов» изображен на фиг. 197; можно считать, что он лежит под кремнекислородным слоем, изображенным на фиг. 196. Атомы Са, К и F лежат в плоскости симметрии, а остальные атомы располагаются по обе стороны от этой плоскости. «Активные» атомы кислорода двух противолежащих слоев соединены четырьмя атомами кальция. Атом фтора находится в свободном промежутке внутри каждой группы из четырех атомов кальция. Атом калия размещается в большой полости, окруженной группой из восьми молекул воды. Подобные полости располагаются непосредственно под центральным четырехчленным кольцом, показанным на фиг. 196; вершины всех тетраэдров этого кольца смотрят вверх.
Совершенная базальная спайность, параллельная (091), по-видимому, проходит между кремнекислородными слоями.
Каждый атом кальция находится в семерной координации относительно четырех активных атомов кислорода, двух групп ОН или Н2O и одного атома фтора. Каждый активный кислород соединен с двумя атомами кальция и одним атомом кремния.
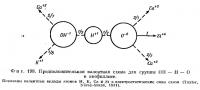
Особый интерес представляет окружение атомов калия. Если считать, что это окружение образовано нейтральными молекулами Н2O, то правило Паулинга о полной компенсации валентностей не будет соблюдаться даже приблизительно. Во-первых, нейтральная молекула Н2O в этом случае получила бы 2/7 валентности от атома Са и 1/8 от атома К (фиг. 198). Во-вторых, атом кислорода получил бы только 1 + 2/7 + 2/7 (= 11/7) валентности, тогда как для полной компенсации необходимо 2 валентности. Кроме того, атомы О-2 не лежат в плоскости атомов Si, Са, с которыми они связаны, но смещены из этой плоскости по направлению к предполагаемым группам Н2O. С другой стороны, правило Паулинга соблюдается и отмечаемое смещение атомов кислорода находит объяснение, если считать, что описываемая координационная группа вокруг атомов К состоит не из молекул Н2O, а из групп ОН~, а дополнительные атомы водорода размещаются между группами ОН- и О'2. При этом сумма валентностей составляет для кислорода 1 + 2/7 + 2/7 + 1/2 = 29/14, или приблизительно 2, а для ОН- 1/2 + 27 + 1/8 = 51/56, или приблизительно 1.
Конфигурация ОН — Н — О является промежуточной между молекулой воды и гидроксильной группой. Процесс дегидратации, при котором теряется большая часть воды, протекает в области температур близ 250° С, т. е. близ температуры, промежуточной между температурами, при которых происходит потеря несвязанной воды и ионов гидроксила. Для более четкого представления об этой структуре необходимо провести непосредственное определение положений атомов водорода с помощью одного какого-либо из известных в настоящее время методов.
Литература по структурам минералов, не описанных в тексте